自身免疫病是第三大常见的疾病类别,仅次于癌症和心脏病。值得关注的是,80%的自身免疫病患者是女性,例如,在系统性红斑狼疮(SLE)中,女性与男性患者的比例为9:1,在干燥综合征(Sjögren's disease)中,女性与男性患者的比例更是高达19:1。
男性与女性之间核心差异在于性染色体的不同,女性拥有两条X染色体(XX),男性则有一条染色体和与之配对的一条Y染色体(XY),克氏综合征患者(XXY)由于具有Y染色体而属于男性,实际上其表型和激素模式也表现为男性,但其与女性的自身免疫病风险相同,这提示了我们,X染色体的数量似乎是自身免疫病风险的主要驱动因素,无论其性别或激素状态如何。此外,同卵双胞胎显示出不同的自身免疫病发病率,这表明除了遗传易感性之外,环境因素也可能是自身免疫病发展的驱动因素。
X染色体中的一个长链非编码RNA(lncRNA)——Xist,只在雌性细胞中表达,以随机失活雌性两条X染色体中的一条,以保证雌性和雄性细胞中基因数量大体相同。
2024年2月1日,斯坦福大学张元豪团队在 Cell 期刊发表了题为:Xist ribonucleoproteins promote female sex-biased autoimmunity 的研究论文。
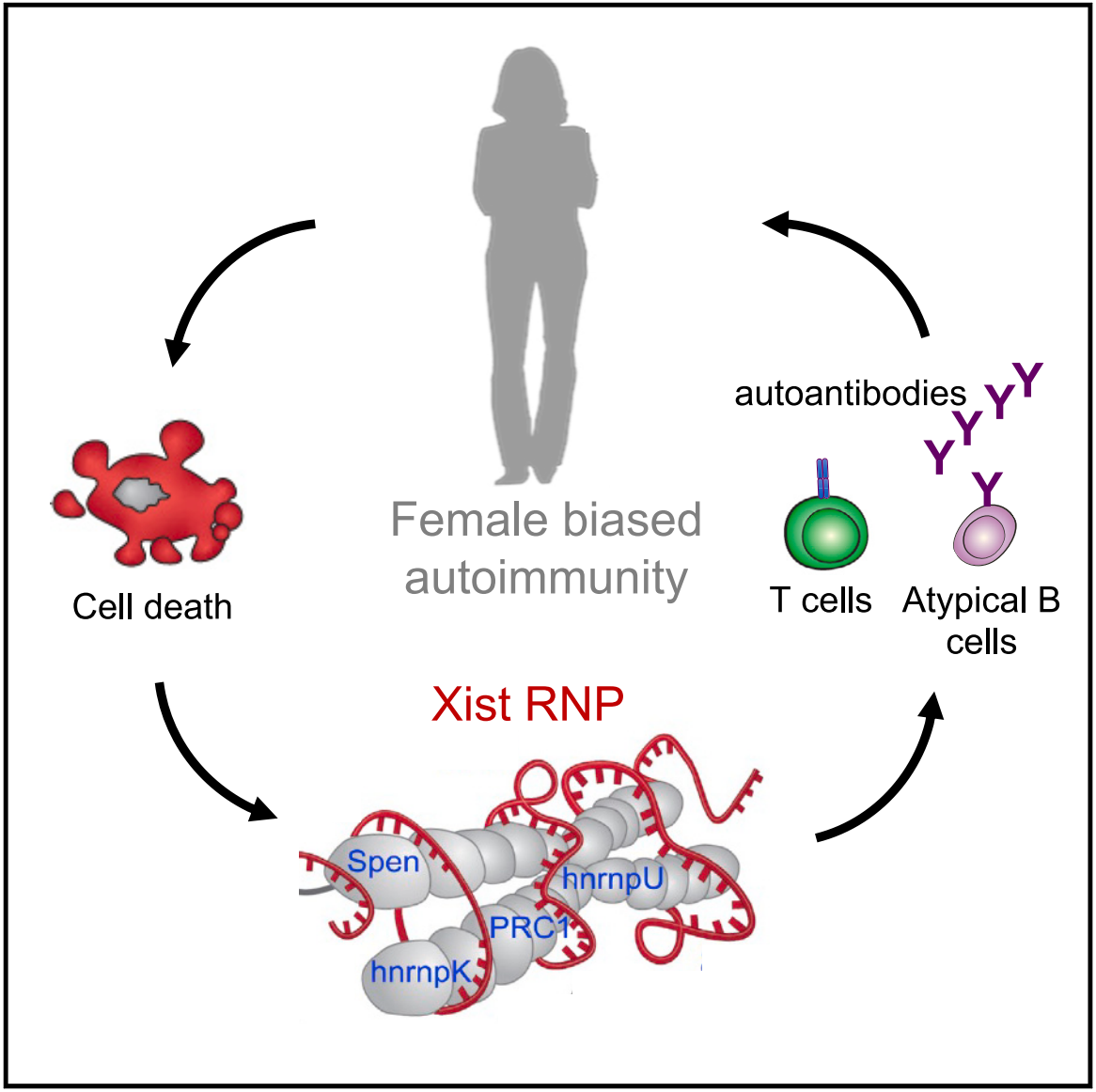
女性的两条X染色体会随机失活一条,该研究表明,调控雌性的X染色体中的一条随机失活的长链非编码RNA(lncRNA)——Xist,其与多种RNA结合蛋白结合形成XIST-RNP,其包含的多种自身抗原成分导致了自身免疫。由于Xist只在人类和雌性哺乳动物细胞中表达,因此驱动了性别偏倚自身免疫。

不只是人类,整个哺乳动物界的雌性都是XX染色体,雄性则是XY染色体。Y染色体只携带了少量基因,没有Y染色体也可以过上完整的人生,实际上,地球上有一半的人(女性)没有Y染色体,她们一样生活的很好。但无论是人类还是其它哺乳动物,都不能在没有X染色体的情况下存活。
X染色体携带了数百个编码蛋白的基因,女性比男性多一条X染色体,这可能会导致女性细胞中蛋白质表达增加,这种过量的蛋白表达将是致命的。而大自然设计了一个聪明而有复杂的方法来解决这一问题——X染色体失活,在胚胎发育早期,哺乳动物的每个细胞都会独立做出决定,随机关闭两个X染色体中的一个,从而保证了女性和男性的细胞中表达蛋白的基因数量大体上相同。
雌性身体中的每个细胞通过长链非编码RNA(lncRNA)——Xist的作用,在表观遗传上沉默两个X染色体之一。Xist长度约19kb(在小鼠中约17kb),仅从失活的X染色体中转录,因此,在雄性中不表达。
在小鼠胚胎干细胞中建立X染色体失活(XCI)期间,Xist与81个独特的结合蛋白结合形成核糖核蛋白复合物(XIST RNP),其中10个通过直接RNA-蛋白相互作用,其他通过间接的蛋白质-蛋白质相互作用,而一些Xist结合蛋白曾被认为是自身抗原。XIST RNP由lncRNA与RNA结合蛋白组成,并与基因组DNA片段相连,具有类似于核酸-自身抗原免疫复合物的特性。
为了研究XIST RNP在自身免疫倾向中的影响,不依赖于性染色体或激素背景,我们利用可诱导和非沉默的Xist等位基因,在自身免疫耐受的C57BL/6J和自身免疫倾向的SJL/J菌株背景中引入常染色体。
为了研究XIST RNP在独立于性染色体或激素背景的自身免疫倾向的影响,研究团队在自身免疫抗性的C57BL/6J小鼠和自身免疫易感性的SJL/J小鼠中,将XIST的诱导和非沉默等位基因引入常染色体中。在雄性小鼠中诱导转基因Xist RNP形成,使用化学诱导剂Pristane诱导的系统性红斑狼疮(SLE)模型,在雄性背景下研究这种雌性特异性lncRNA。
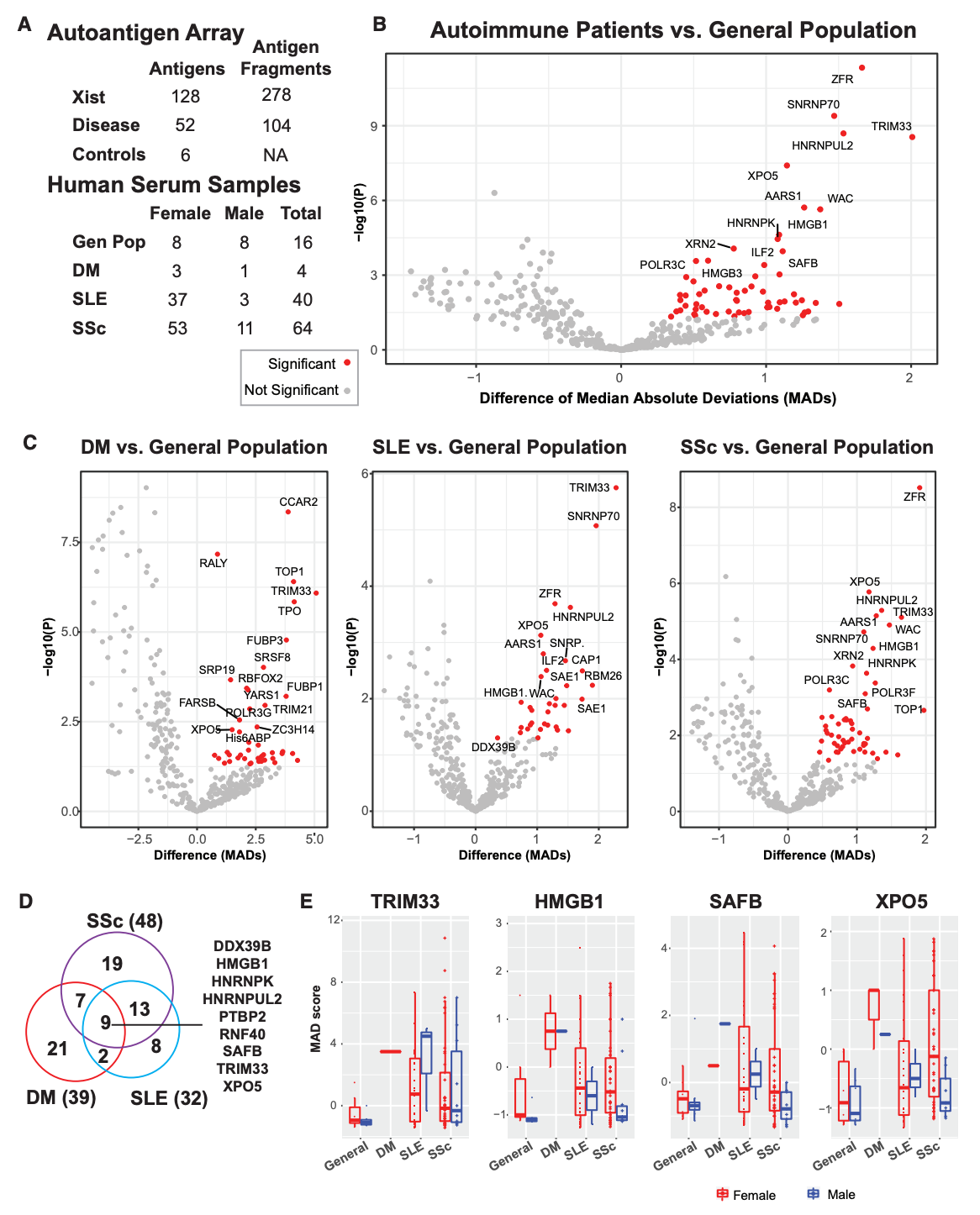
结果显示,在化学诱导剂Pristane诱导的系统性红斑狼疮(SLE)小鼠模型中,表达转基因Xist的雄性SJL/J小鼠比野生型雄性小鼠表现出更严重的多器官病理。雄性小鼠中的Xist表达重编程了T和B细胞群以及染色质状态,使其更类似于野生型雌性小鼠。研究团队还设计了一种抗原阵列来测试自身免疫患者对XIST RNP的血清活性,检测到人类自身免疫病患者对XIST RNP的多个组分的显著反应性。
论文链接:







发表评论 取消回复