2023年5月12日国家药监局发布了《国家药监局综合司关于2023年医疗器械行业标准制修订计划项目公示》根据《医疗器械标准管理办法》《医疗器械标准制修订工作管理规范》要求,确定了2023年117项医疗器械行业标准制修订计划项目(具体项目名单见文末)。
此次公布的计划名单中,强制性行业标准制修订项目计划共有15项(见文末附件1)。
其中,医用电气设备 第2-87部分:高频呼吸机的基本安全和基本性能专用要求这1项,根据国际标准进行新的行业标准制定;
其余电动洗胃机、血压传感器、骨接合植入器械 金属接骨螺钉、接骨板等14项在现有行业标准基础上进行修订。
推荐性 行业标准制修订项目计划共有102项,其中56项为推荐根据国际标准进行新的行业标准制定,46项为在现有行业标准基础上进行修订。
修订最新的医疗器械行业标准的目的主要是为了:
加强医疗器械产品的质量控制,提高用户体验和安全性。
统一医疗器械行业的技术标准和规范,推动行业技术进步和创新。
增强医疗器械行业的竞争力,促进行业健康发展。
对企业来说,新的医疗器械行业标准会直接影响到产品研发、生产、销售等环节。企业需要对新的标准进行了解和理解,按照标准要求进行产品设计、制造和销售。如果企业无法满足新标准要求,就可能受到批评、处罚和市场竞争的影响。
另一方面,新标准的引入也会带来机遇。企业可以利用新标准提供更好、更安全的医疗器械产品,增强市场竞争力和用户口碑,促进企业发展。
22个标准项目,由企业牵头制修订!
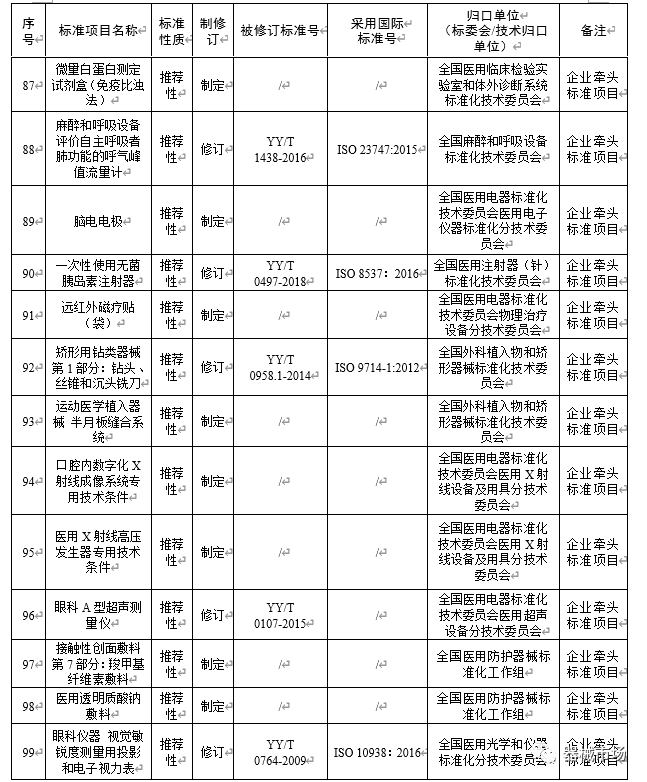
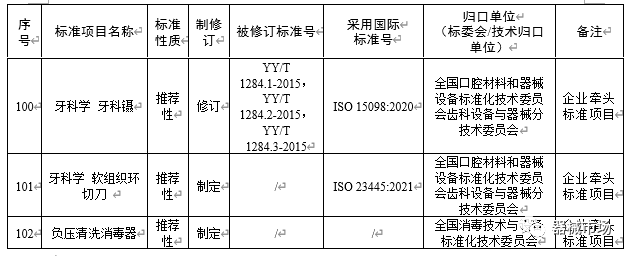
值得注意的是,在本次发布的推荐性行业标准制修订项目计划中,22个项目备注为: 企业牵头标准项目(见下表)。
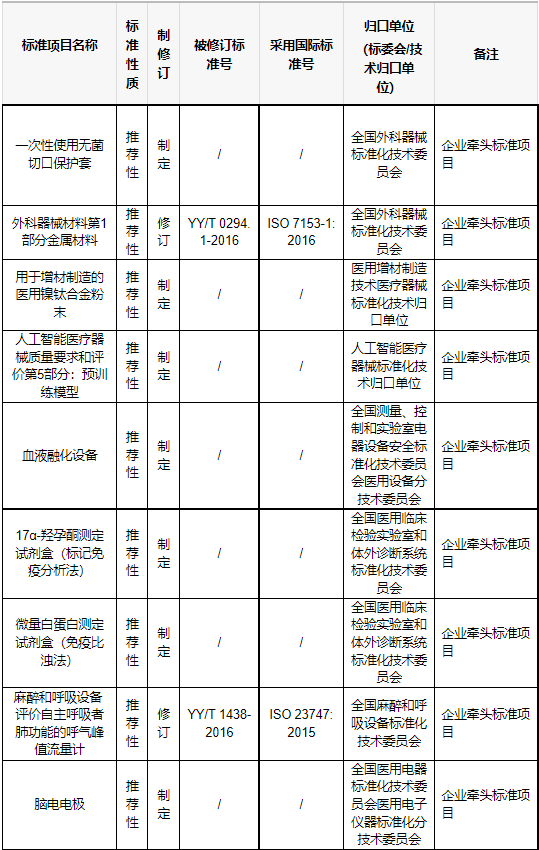
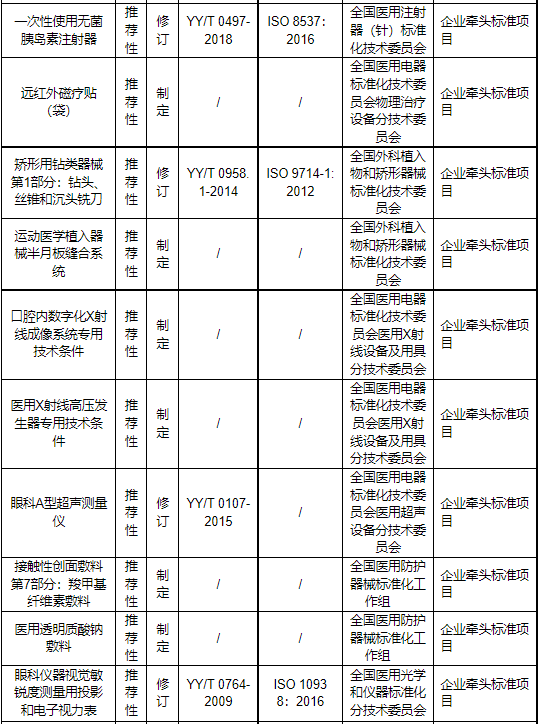
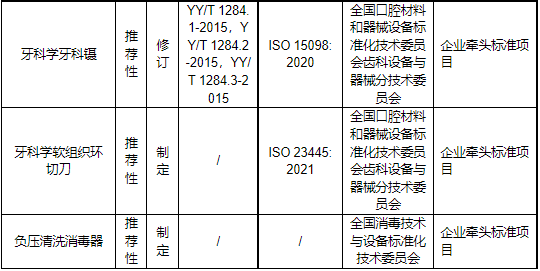
通常情况下,医疗器械推荐性行业标准由行业协会、专业委员会、科研机构等组织牵头起草,但对于企业来说,如果它们是某项医疗器械的主要生产、销售企业,或拥有某项先进技术或特殊经验的企业,则可能会被邀请参与制定该医疗器械的标准。
企业牵头起草医械行业标准有工作规范啦!
就在2023年4月24日,国家药监局医疗器械标准管理中心发布通知:
为鼓励以企业为主体牵头起草医疗器械推荐性行业标准的积极性,促进医疗器械标准供给更加优质、及时、多元,根据《医疗器械标准管理办法》《医疗器械标准制修订工作管理规范》等有关规定,制定了《企业牵头起草医疗器械推荐性行业标准工作规范(试行)》。

对于企业来说,能够参与起草医疗器械行业标准绝对是益处多多,比如说:
可以提高企业的声誉,彰显企业在技术、品质等方面的实力和专业性。
对企业的技术水平、创新能力、市场洞察力等提出更高要求,促进企业自我完善。
能够深入了解和掌握当前行业的技术动态、政策动向以及市场趋势,为企业的战略发展提供有益的参考。
为企业提供了与其他行业专业人士、学术机构、政府部门等合作的机会,有助于扩大企业的交流合作网络。
总的来说,参与起草医疗器械推荐性行业标准可以让企业更好地了解市场需求和发展趋势,提高企业在行业中的竞争力和市场份额,同时也能为整个行业的技术水平提供推动力,进一步促进行业发展。
附件1:2023年医疗器械强制性行业标准制修订项目计划
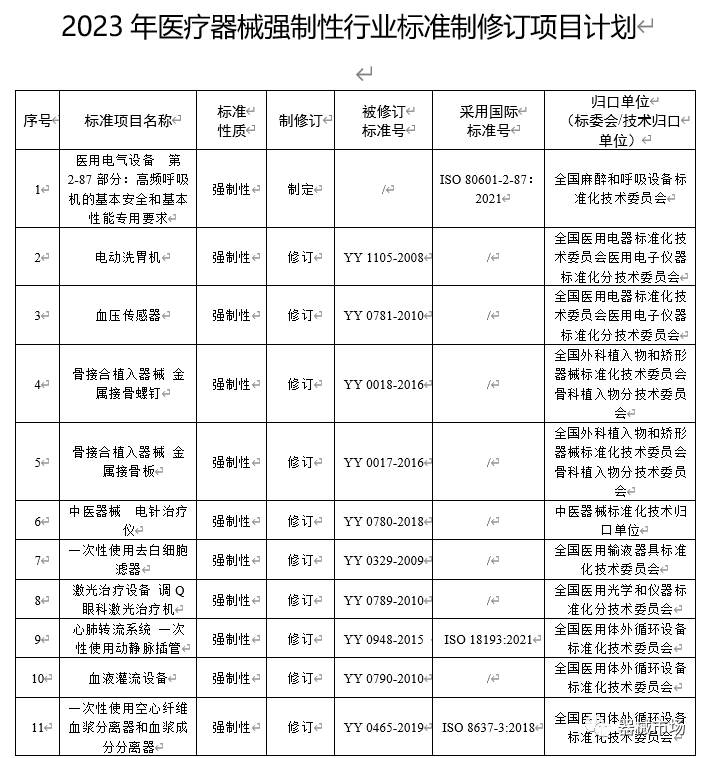
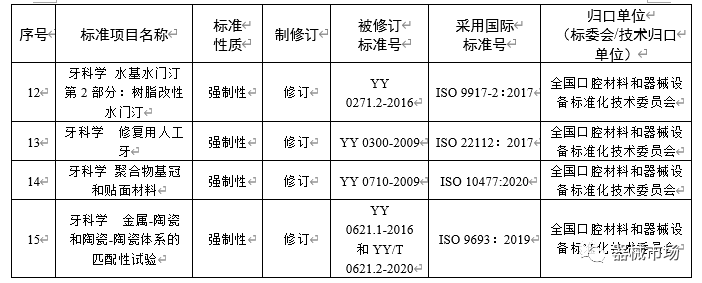
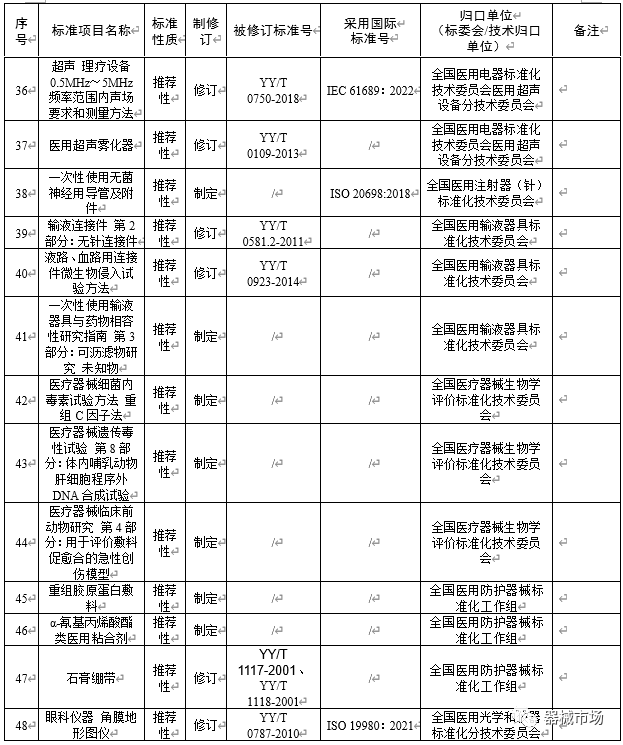
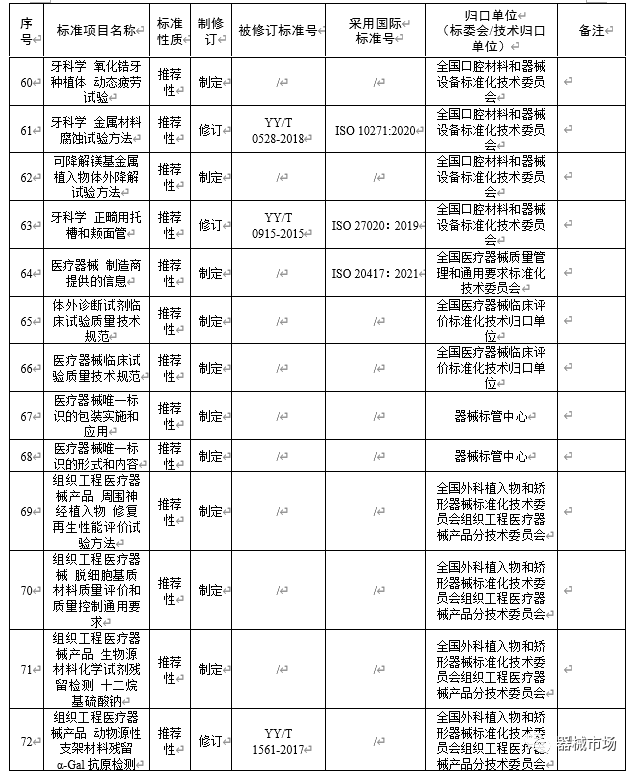
附件2:2023年医疗器械推荐性行业标准制修订项目计划
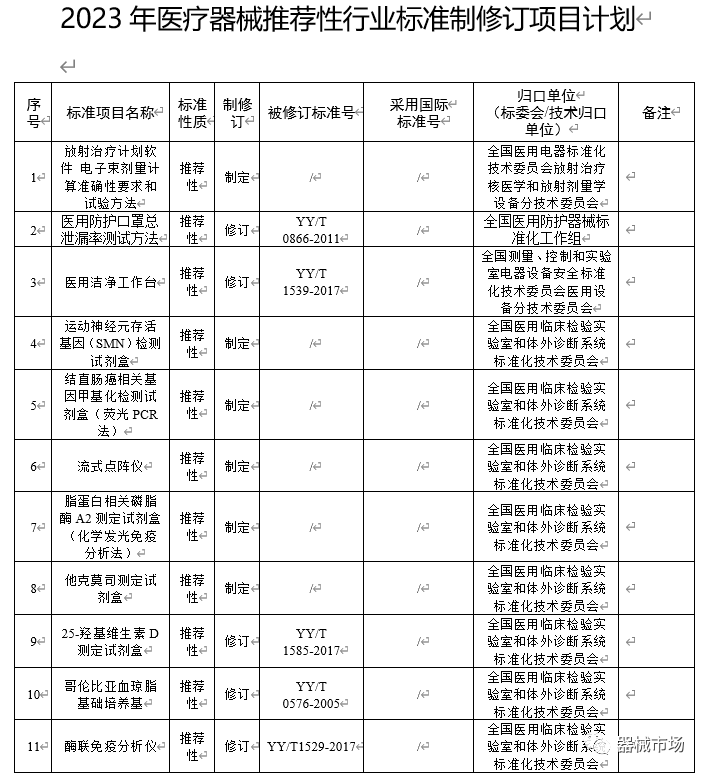
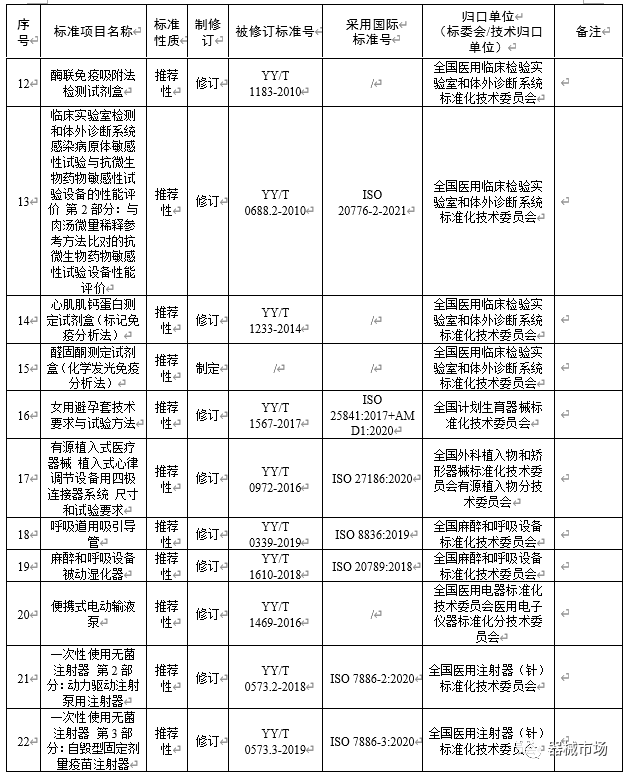
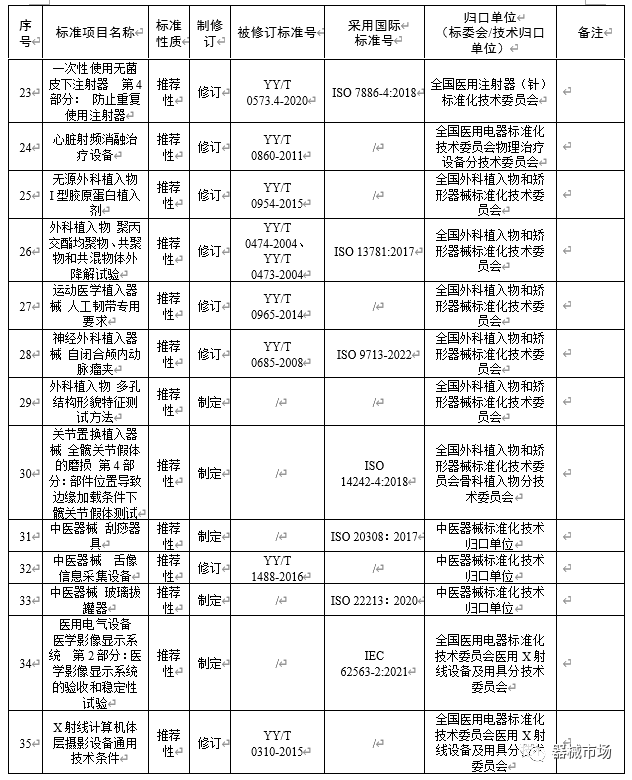


END







发表评论 取消回复