卵巢癌作为具有高度隐匿性的妇科恶性肿瘤,特别是当进入铂耐药阶段后,患者缺少有效治疗药物,预后极差。索米妥昔单抗(MIRV,Mirvetuximab Soravtansine)作为全球首个获批用于卵巢癌治疗的抗体偶联药物(ADC),能够通过特异性识别叶酸受体α(FRα)阳性的肿瘤细胞实现精准打击。近日索米妥昔单抗III期确证性临床研究MIRASOL研究全文正式发表于顶级期刊《New England Journal of Medicine》,IF:72.406,标志着索米妥昔单抗已正式获得学术界的认可,卵巢癌治疗进入ADC时代。以下将带来该文献的全文解读。

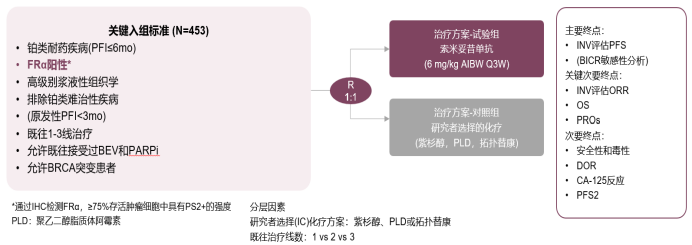
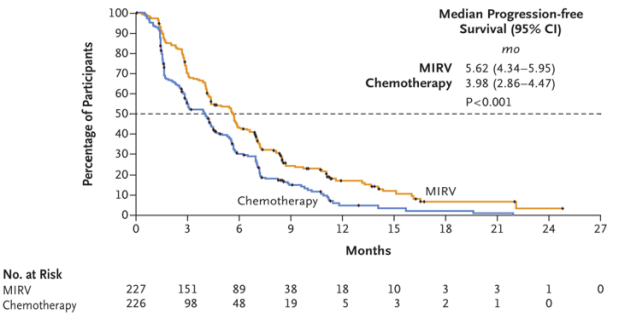
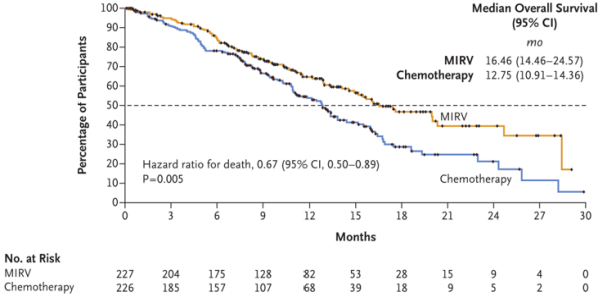
MIRASOL研究是一项国际多中心、随机对照、确证性的III期临床研究,旨在比较索米妥昔单抗和研究者选择的化疗在FRα高表达的PROC患者中的疗效和安全性。入组患者按照1:1的比例随机分配进入索米妥昔单抗组(6mg/kg Q3w AIBW)和研究者选择的化疗组(紫杉醇、PLD、拓扑替康),直至出现疾病进展或不可耐受的毒性。主要研究终点为研究者评估的PFS,次要终点包括研究者评估的ORR、OS、患者报告结局、DOR、PFS2、CA125缓解率和安全性。该研究自2020年2月3日正式启动,初步数据分析截至2023年3月6日。该研究共纳入453例高级别浆液性、既往接受过1-3线系统治疗、FRɑ阳性的PROC患者,排除铂难治性患者。227例患者接受索米妥昔单抗治疗,226例接受研究者选择的化疗。总共425例患者接受了至少一次治疗(索米妥昔单抗组218例,研究者选择的化疗组207例),纳入安全性分析。分层标准包括BRCA突变状态、既往接受系统治疗线数、既往治疗方案等。从患者基线特征来看,87%的患者既往接受过2-3线系统治疗。索米妥昔单抗组对比研究者选择的化疗组的中位治疗持续时间为4.98个月(7个治疗周期)vs 2.96个月(3个治疗周期)。疗效方面,索米妥昔单抗相较化疗显著改善FRα高表达PROC患者长期生存,降低35%的疾病进展风险(mPFS: 5.62 vs 3.98 月, HR=0.65, P<0.0001 )和33%的全因死亡风险(mOS: 16.46 vs 12.75 月, HR=0.67, P=0.0046)。同时,索米妥昔单抗可显著改善患者的PFS2,能够降低37%的二次疾病进展风险(PFS2: 11.04 vs 8.05 月, HR=0.63)主要研究终点:无疾病进展生存时间(PFS,Progression-free Survival)关键次要终点:总生存时间(OS,Overall Survival)次要研究终点:至二次疾病进展或死亡时间(PFS2, Second progression-free survival)索米妥昔相比化疗能够极大的提升患者的客观缓解率(ORR: 42.3% vs 15.9%,索米妥昔组包括12例CR和84例PR)和CA125缓解率(58% vs 30.3%),并且延长缓解持续时间(mDOR: 6.77 vs 4.47 月)。另亚组分析显示,索米妥昔单抗在各亚组获益基本保持一致,均优于化疗,其中:•BRCA突变阳性、既往经PARP抑制剂或多柔比星治疗、既往经系统治疗线数更少的患者接受索米妥昔单抗治疗获益更明显;•无论既往是否接受过贝伐珠单抗治疗,索米妥昔单抗相较化疗均可显著改善患者的PFS。(未接收贝伐珠单抗治疗患者HR=0.66, P=0.02;贝伐珠单抗治患者HR=0.64, P=0.0011 )。PFS、OS亚组分析
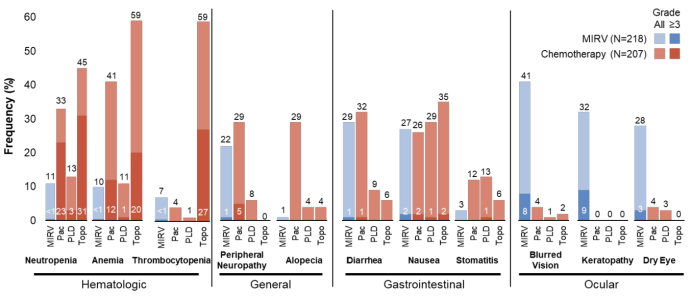
安全性分析显示,索米妥昔单抗的毒性主要为眼毒性及胃肠道毒性。索米妥昔单抗与化疗相比, 3级及以上不良事件发生率、严重不良事件(SAE)发生率及停药率均更低(41.7% vs 54.1%,23.9% vs 32.9% ,9.2% vs 15.9%),并且血液学不良事件发生率也明显低于化疗,安全性更优。眼部AE是抗微管ADC类药物的常见不良事件,MIRASOL研究中56%的患者发生眼部AE,3级及以上AE的发生率为14%,随访中几乎所有的AE均可缓解至0或1级,仅4例患者因眼部不良事件停止治疗。研究中未发现患者出现角膜溃疡或穿孔,无患者遗留永久性眼部后遗症。MIRASOL研究结果表明,索米妥昔单抗疗效更优且更安全,已经超越了传统化疗成为FRα阳性铂耐药卵巢癌患者的标准治疗。在亚组分析中,研究显示无论BRCA突变状态和前线接受何种治疗方案,索米妥昔单抗均较化疗体现生存优势,且早线患者相较后线患者获益更多。索米妥昔单抗目前已获得NCCN卵巢癌指南2023版、NCCN卵巢癌指南2023中文版、CSCO卵巢癌指南2023版、CSGO卵巢癌指南2023版等多个国内外权威指南的推荐,单药或联合贝伐珠单抗用于FRα阳性的PROC患者。尽管索米妥昔单抗尚未在国内正式获批,但为了尽早惠及国内患者,借助国家政策支持,瑞金医院海南医院自去年7月起已成功引入药物,方便国内患者赴岛内接受检查和治疗。当前索米妥昔单抗为基础的多项联合治疗研究也正在积极探索中,例如联合贝伐珠单抗在铂敏感复发2L维持治疗的 III期随机对照临床研究GLORIOSA 预计将于近期在国内正式启动入组,有望进一步的帮助卵巢癌的早线患者。以终为始,以始为终,新英格兰的登顶,将激励索米妥昔单抗在卵巢癌的进一步探索,为战胜疾病继续努力。
1.Moore KN, et al. N Engl J Med. 2023 Dec 7;389(23):2162-2174.













发表评论 取消回复