多省药监局飞检!大批械企被查
12月27日,福建省药监局发布了对40家医疗器械企业的飞检结果公告,其中7家企业被要求停产整改,28家企业在质量管理体系方面发现一般性缺陷;另有5家企业在飞行检查时已处于停产状态。
福建省药监局此次飞检,不仅涉及大博医疗这类上市械企,还在检查过程中发现大量问题:

实际上,就在12月,上至国家,下至各省,都密集开始医疗器械飞检,大批械企被停产整改。
今年12月,内蒙古赤峰市市场监督管理局发布《2023年医疗器械经营企业飞行检查情况公示》。29家械企被查出存在缺陷,并被责令限期整改。
同样在12月,山东省药监局对全省128家重点监管医疗器械生产企业开展了合规检查,对12家医疗器械生产企业开展了飞行检查,对8家医疗器械生产企业开展了专项检查。
其中济宁市健达医疗器械科技有限公司、山东煜和堂药业有限公司、济南康民药业科技有限公司3家企业被停产整改。
无独有偶,12月11日,云南省药监局对6家医疗器械生产企业开展了飞行检查。检查中共发现49项缺陷。其中云南众乾义齿科技有限公司和云南好迪医疗器械有限公司两家械企被查出多项关键不符合项,被责令停产整改。
同样在12月,国家药监局发布公告,组织检查组对上海舍成医疗器械有限公司、成都市新兴内窥镜科技有限公司进行飞行检查,发现2家企业质量管理体系存在严重缺陷。
国家药监局要求企业完成全部缺陷项目整改,并经属地省级药品监督管理部门复查合格后方可恢复生产。
全国性文件下发:今年这些器械被查
在全国药监局密集飞检背后,是国家药监局今年对医疗器械质量监管的严格要求。
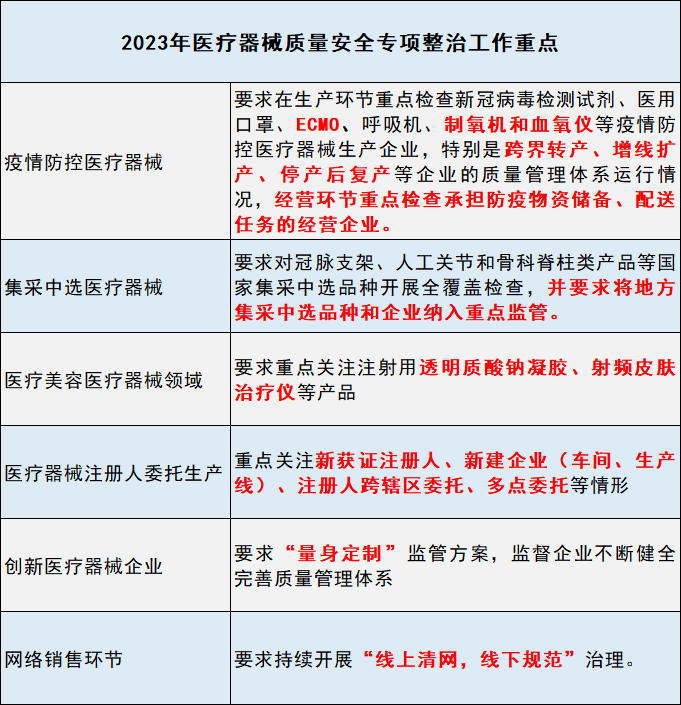
早在今年2月,国家药监局发布了《关于开展2023年医疗器械质量安全专项整治工作的通知》。
 此份文件明确,2023年专项整治工作围绕十个方面重点任务推进,重点突出,手段多样,方向明确。
此份文件明确,2023年专项整治工作围绕十个方面重点任务推进,重点突出,手段多样,方向明确。
涵盖疫情防控医疗器械、集中带量采购中选医疗器械、无菌和植入性医疗器械等重点产品;
医疗器械注册人委托生产、创新医疗器械企业、生产经营重大变化企业等重点企业;
特定人群使用医疗器械、网络销售等重点环节和医疗美容医疗器械以及严查违法违规行为等重点领域;
2023年的专项整治,在去年专项整治的基础上,整治范围全面扩大,整治重点更加突出。对于各项重点任务明确了生产、经营、使用各环节重点关注情形和检查重点等具体要求。
 国家局突袭!境外医疗器械企业被停产
国家局突袭!境外医疗器械企业被停产
除了境内医疗器械企业,药监局也加强了对境外医疗器械企业及产品的检查。
国家药监局今年相继发布两则公告,对境外医疗器械企业开展远程非现场检查,相关企业产品被暂停进口、经营和使用。
9月,对韩国普瑞斯特医疗有限公司盆腔脏器脱垂修复系统(注册证号:国械注进20183182310)进行检查,发现,该产品生产过程存在实际生产工艺与生产工艺流程图不一致、未按照经注册的产品技术要求开展检测等问题。
10月,对瑞典科沃医疗科技有限公司肺脏灌注系统(注册证号:国械注进20233100363)进行检查,发现,该产品存在生产地址与注册证载明信息不一致等问题。
实际上,无论是飞检还是抽检,境外还是境内,药监局今年都加大了针对医疗器械的检查力度,对于企业以及广大经销商而言,只有针对生产、销售、贮存、运输全流程进行更为细致的自查,才能够防患于未然。







发表评论 取消回复